Perfis de Paciente: Caroline, 40 anos
9 motivos para se vacinar contra cânceres, verrugas genitais e outras doenças causadas pelo HPV.1
Caroline, 40 anos de idade.
Mãe de 2 filhos, diagnosticada com
neoplasia intraepitelial cervical.
Ela vem buscando entender a doença.

Personagem meramente fictício.
A proporção de lesões NIC 2+ (NIC 2/NIC 3/AIS) atribuíveis aos tipos de HPV 31/33/45/52/58 aumentou com a idade e foi significativamente maior entre as mulheres de 35 a 39 anos em comparação com as mais jovens; p < 0,001.2
Atribuição proporcional dos genótipos de HPV entre mulheres diagnosticadas com NIC 2, NIC 3 e AIS2


O genótipo do HPV foi identificado em tecidos de mulheres dos EUA de 21 a 39 anos de idade diagnosticadas com NIC 2/3 e AIS (NIC 2+) através de PCR de consenso L1 e hibridação específica por tipo (projeto HPV-IMPACT). A atribuição do tipo foi estimada usando pesos para contabilizar as lesões.²
NIC: neoplasia intraepitelial cervical.
AIS: adenocarcinoma in situ.
Detalhes do estudo
Características selecionadas entre mulheres diagnosticadas com NIC 2+ pelo status de tipagem do DNA do HPV
| SIM | NÃO | |
| N (%) | N (%) | |
| Total Diagnóstico | 5.378 (63,3) | 3.112 (36,7) |
| NIC 2 | 2.678 (49,8) | 1.510 (48,5) |
| NIC 2/3 | 870 (16,2) | 543 (17,4) |
| NIC 3/AIS | 1.830 (34,0) | 1.059 (34,0) |
| Faixa etária, anos | ||
| 18-20 | 325 (6,0) | 152 (4,9) |
| 21-29 | 3.218 (59,8) | 1.821 (58,5) |
| 30-39 | 1.835 (34,1) | 1.139 (36,6) |
| Raça/etnia | ||
| NH branca | 2.881 (62,0) | 1.432 (58,7) |
| NH preta | 792 (17,0) | 411 (16,8) |
| Hispânica | 651 (14,0) | 404 (16,6) |
| Asiática | 207 (4,5) | 89 (3,6) |
| Outra | 117 (2,5) | 105 (4,3) |
| Desconhecido | 730 | 671 |
| Seguros | ||
| Privado | 3.009 (64,2) | 1.578 (61,1) |
| Público | 1.308 (27,9) | 798 (30,9) |
| Sem seguro | 164 (3,5) | 100 (3,9) |
| Outro | 204 (4,4) | 105 (4,1) |
| Desconhecido | 693 | 531 |
| Estado vacinal | ||
| Vacinada | 961 (36,2) | 383 (32,8) |
| Não vacinada | 1.691 (63,8) | 785 (67,2) |
| Desconhecido | 2.726 | 1.944 |
Adaptado de: Hariri S et al.²
Analisar a atribuição de HPV carcinogênico em amostra de mulheres dos EUA diagnosticadas com NIC 2, NIC 3 e AIS e estimar o impacto potencial da vacina nonavalente em lesões de NIC 2+ por idade e raça/etnia.²
De 2008 a 2011, um total de 8.490 mulheres com idades entre 18 e 39 anos, diagnosticadas com NIC 2+ não invasivo, foram registradas no sistema de monitoramento HPV-IMPACT. Amostras arquivadas foram recuperadas para 6.177 (72,8%) das mulheres diagnosticadas, das quais 5.401 (87,4%) foram consideradas histologicamente adequadas e passaram por teste de DNA. Resultados de DNA do HPV foram obtidos para 5.378 (99,6%) das mulheres testadas.²
O HPV foi tipado em tecidos arquivados de mulheres com idades entre 21 e 39 anos, residentes em cinco áreas de abrangência nos Estados Unidos, que tinham NIC 2/3 e AIS (NIC 2+). Para tal, utilizou-se PCR de consenso L1 e hibridização específica para cada tipo de HPV. A atribuição do tipo foi estimada usando pesos para levar em conta lesões com múltiplos tipos detectados.²
No geral, 75% das lesões foram atribuíveis a 7 tipos oncogênicos de HPV: 50% aos HPV 16 e 18, e 25% aos genótipos 31, 33, 45, 52 e 58. Os tipos de HPV 16 e 18 tiveram a maior fração atribuível à NIC 2+ em todas as subpopulações, embora em menor extensão em mulheres mais velhas e minorias raciais/étnicas.²
O risco de desenvolvimento de cânceres e pré-malignidades associados ao HPV está fortemente relacionado ao diagnóstico de NIC 3.³

O risco aumentado em longo prazo pode ser explicado pela maior susceptibilidade a novas infecções por HPV de alto risco e pelo agravamento da doença devido à incapacidade de se eliminar completamente a infecção.3
Taxas de incidência estimadas de carcinomas e pré-malignidades relacionados ao HPV, comparando mulheres com e sem histórico de NIC 3.
O primeiro ano após o diagnóstico de NIC 3 ou nevo dérmico benigno foi incluído na taxa de incidência visualizada nesta figura. As barras de erro indicam os intervalos de confiança de 95% das taxas de incidência estimadas. Os asteriscos indicam uma diferença significativa nas taxas de incidência do grupo com histórico de NIC 3 em comparação com o grupo sem histórico de NIC 3.
No Brasil, a vacina nonavalente contra o HPV está indicada para a prevenção dos cânceres de colo do útero, vulva, vagina e ânus causados pelos tipos de HPV 16, 18, 31, 33, 45, 52 e 58; e de verrugas genitais causadas pelos tipos 6 e 11.¹
NIA: neoplasia intraepitelial anal; NIV: neoplasia intraepitelial vulvar; NIVA: neoplasia intraepitelial vaginal.

89.018
mulheres com diagnóstico de NIC 3 prévio e 89.018 controles pareados sem história de NIC 3.³

O objetivo desse estudo foi determinar o risco de carcinomas e pré-malignidades relacionados ao HPV em mulheres diagnosticadas com NIC 3.³

Mulheres diagnosticadas com NIC 3 entre 1990 e 2010 foram identificadas no registro nacional de histopatologia e citopatologia dos Países Baixos (PALGA) e combinadas com um grupo de controle de mulheres sem NIC 3. Posteriormente, todos os casos de lesões de alto grau associadas ao HPV de alto risco e de carcinomas na região anogenital e na orofaringe entre 1990 e 2015 foram extraídos. Foram estimadas as razões de taxa de incidência de carcinomas e prémalignidades de vulva, vagina, ânus e orofaringe.³
Estudos demonstraram que a vacinação pode contribuir para a prevenção de recidiva de NIC em mulheres com HPV positivo e tratadas com conização.⁴
A vacinação contra o HPV contribuiu para:
- Redução de 59% no risco de desenvolvimento de novas lesões epiteliais cervicais de grau 2+.⁴
- Nos casos de NIC 2+ positivos para os HPV 16/18, houve redução de 63% no risco de recorrência.⁴
A vacinação contra o HPV contribui para a redução no desenvolvimento de novas lesões intraepiteliais cervicais.4
Estudo de vacinação profilática contra o HPV após a conização: uma revisão sistemática e meta-análise
Incluídas 21.059 pacientes (3.939 vacinadas versus 17.150 controles).4
Todas as pacientes, independentemente do tipo de HPV.4

Adaptado de: Jentschke M, et al.4
- Redução significativa de 59% no risco de desenvolvimento de novas lesões epiteliais cervicais de grau 2+ após a vacinação contra o HPV.4
- A análise dependente da idade não mostrou diferenças entre mulheres com menos de 25 anos (RR = 0,47, IC de 95% = 0,28; 0,80) e mulheres com idade superior (RR = 0,52, IC de 95% = 0,41; 0,65).4
- Resultados de NIC 2+ positivos para HPV 16/18 mostraram uma RR de 0,37 (IC de 95% = 0,17; 0,80) = redução no risco de 63%.4
- Não houve diferença significativa entre os grupos que receberam a vacinação antes ou depois da conização.4
- Estudos publicados de 2012 a 2020.⁴
- Dez estudos, que envolveram 21.059 pacientes, foram incluídos após a consideração dos critérios de inclusão e exclusão.⁴
- A vacinação contra o HPV foi realizada após tratamento cirúrgico em 6 estudos e, antes, em 2 estudos, assim como antes ou após a cirurgia em 2 estudos.⁴
- Em 4 estudos, a vacina aplicada foi a quadrivalente; em 2, a bivalente; e em outros 4 estudos, ambas as vacinas foram utilizadas.⁴
- O desfecho primário foi HSIL ou NIC 2+ em todos os estudos.⁴
HSIL: lesão intraepitelial de alto grau.
NIC: neoplasia intraepitelial cervical.
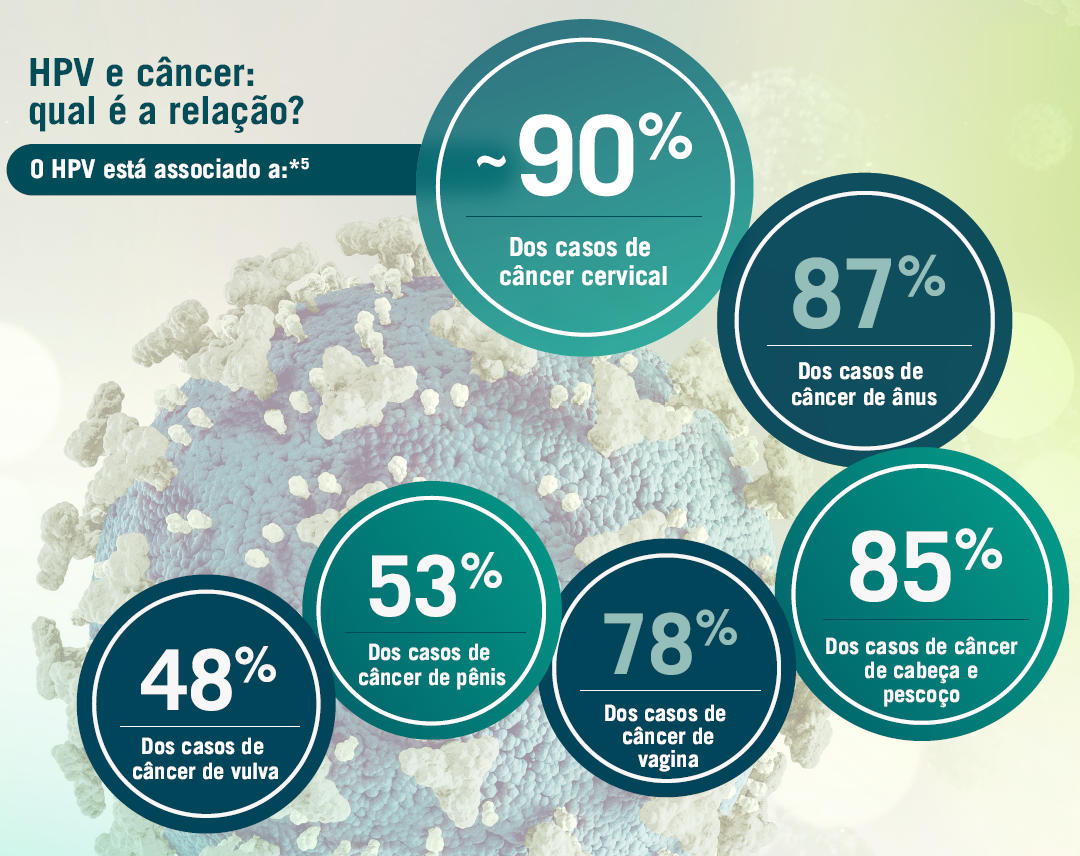
No Brasil, a vacina nonavalente contra o HPV está indicada para a prevenção dos cânceres de colo do útero, vulva, vagina e ânus causados pelos tipos de HPV 16, 18, 31, 33, 45, 52 e 58; e de verrugas genitais causadas pelos tipos 6 e 11.¹
*Dados globais que podem sofrer variações dependendo da região geográfica.
Os genótipos de HPV contidos em GARDASIL 9 estão associados com até 90% dos casos de câncer de colo do útero.5

Adaptado de: WHO5
Referências
- Bula vigente de GARDASIL 9.
- Hariri S, Unger ER, Schafer S et al. HPV type attribution in high-grade cervical lesions: assessing the potential benefits of vaccines in a population-based evaluation in the United States. Cancer Epidemiol Biomarkers Prev. 2015;24(2):393-399.
- Ebisch RM, Rutten DW, IntHout J et al. Long-lasting increased risk of human papillomavirus-related carcinomas and premalignancies after cervical intraepithelial neoplasia grade 3: a population-based cohort study. J Clin Oncol. 2017;35(22):2542-2550.
- Jentschke M, Kampers J, Becker J et al. Prophylactic HPV vaccination after conization: a systematic review and meta-analysis. Vaccine. 2020;38(41):6402-6409.
- World Health Organization (WHO). Weekly epidemiological record. 2022;97(50). Disponível em: https://apps.who.int/iris/handle/10665/365350. Acessado em 02 de agosto de 2023.
Vacina indicada para a prevenção de cânceres, verrugas genitais e outras doenças associadas ao HPV.¹*
*A exemplo de todas as vacinas, a administração da GARDASIL 9 pode não resultar em proteção para todos que a recebem.
As informações requeridas pelo art. 27 da RDC 96/08 (minibula de Gardasil 9) podem ser acessadas clicando aqui.
Ressaltamos que GARDASIL 9 é contraindicado para pessoas com hipersensibilidade a qualquer componente de GARDASIL 9 ou GARDASIL. Terapias imunossupressoras podem reduzir a resposta imunológica às vacinas.
As informações requeridas pelo art. 27 da RDC 96/08 (minibula de Gardasil) podem ser acessadas clicando aqui.
Ressaltamos que GARDASIL é contraindicado para pessoas com hipersensibilidade a qualquer componente do produto. Não existem dados sobre o seu uso concomitante com imunossupressores potentes.
Antes de prescrever os produtos, recomendamos a leitura das bulas completas para informações detalhadas.
SE PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
Material exclusivo para profissionais de sáude habilitados a prescrever ou dispensar medicamentos.
Copyright© 2023 Merck & Co., Inc., Rahway, NJ, EUA, e suas afiliadas. Todos os direitos reservados. BR-HPV-01067.
PRODUZIDO EM AGOSTO/2023. VÁLIDO POR 6 MESES.