Lamina de Vacina Pneumocócica sobre Estudos em Populações Especiais


Seus pacientes pediátricos podem ter risco aumentado de contrair a doença pneumocócica invasiva.1
Condições de risco e alto risco para Doença Pneumocócica Invasiva (DPI)
Avaliação de risco feita com base na presença/ausência de condições médicas que são indicações atuais para vacinação pneumocócica entre crianças e adultos, de acordo com as recomendações estabelecidas pelo ACIP e AAP.2
Taxas de doença pneumocócica invasiva entre crianças <5 anos (casos por 100.000 pessoas-ano)2
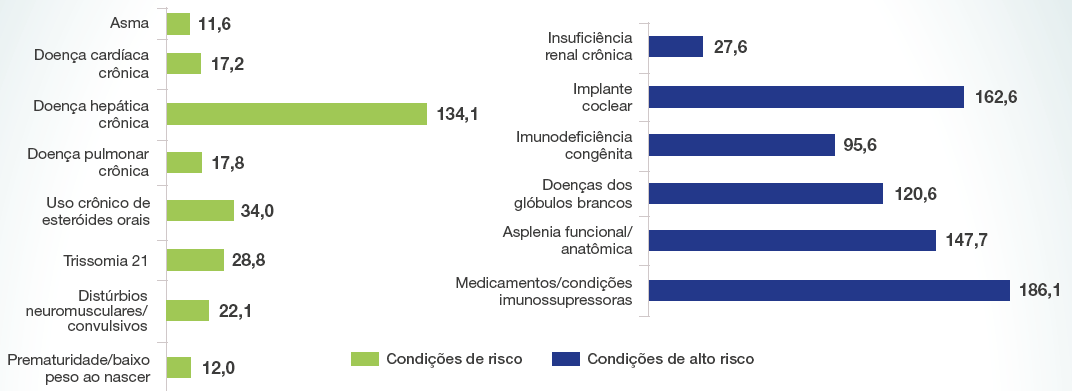
Adaptado de: Pelton SI et al.
ACIP: Comitê Consultivo em Práticas de Imunização; AAP: Academia Americana de Pediatria invasiva.
Incidência de DPI é mais elevada nas crianças < 1 ano de idade em comparação a outros grupos etários3

Coeficiente de incidência de meningite pneumocócica por faixa etária no Brasil entre 2017-2022.3*
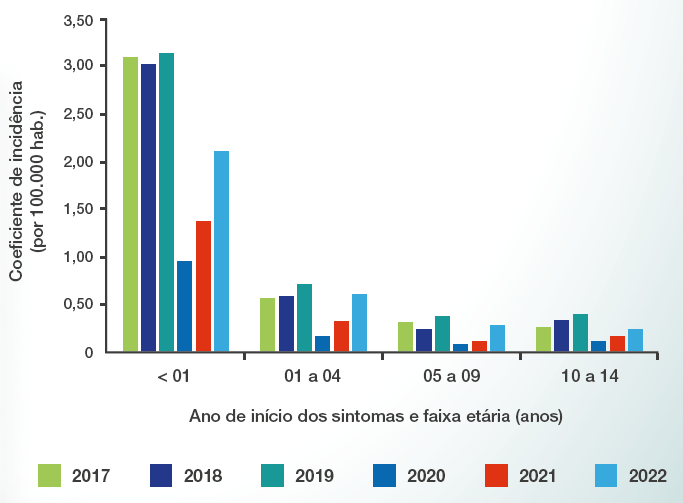
*Dados atualizados em: 27/09/22.3
Adaptado de: Ministério da Saúde.3
O aumento da DPI em crianças é impulsionado pelo sorotipo 34-9
- Apesar da queda geral nos casos de DPI em países com programas nacionais de imunização estabelecidos, o sorotipo 3 ainda é uma ameaça crescente para os pacientes pediátricos.4-6
- O sorotipo 3 é associado a:
- Alto potencial invasivo.7
- Ocorrência de pneumonia complicada.8
- Alto risco de mortalidade.8
- Em 2021 o sorotipo 3 foi uma das principais causas de DPI em crianças menores de 5 anos no Brasil:9*
- ~82% dos casosrelacionados ao sorotipo 3 ocorreram em crianças menores de 1 ano.9
- Segundo sorotipo causador de DPI mais comum em crianças de 0 a 5 anos de idade no Brasil.9
DPI: doença pneumocócica invasiva.
Casos pediátricos de DPI por Sorotipo 3 Europa, 2014-20195
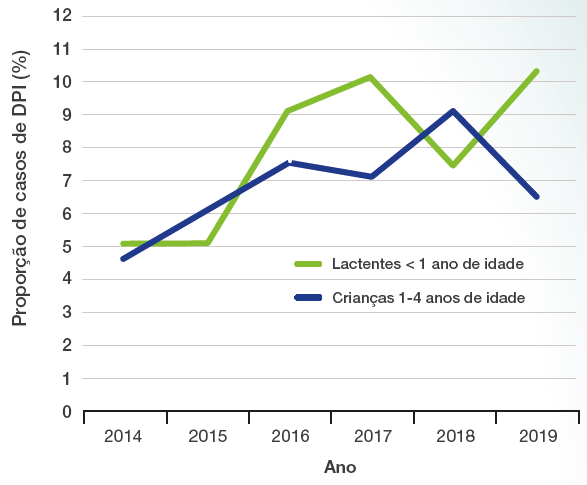
Adaptado de: ECDC.5
VAXNEUVANCE® foi estudado em uma ampla gama de populações pediátricas10,11
Mais de 7.000 bebês e crianças foram incluídos em estudos clínicos para estabelecer a segurança, a tolerabilidade e a imunogenicidade de VAXNEUVANCE®10

Bebês e
crianças saudáveis

Crianças com
doença falciforme

Crianças que
vivem com HIV

Bebês nascidos prematuramente

Crianças que receberam transplante de células-tronco hematopoiéticas alogênico (≥3 anos de idade)
VAXNEUVANCE® demonstrou imunogenicidade em bebês e crianças saudáveis
ou com risco aumentado de doença pneumocócica invasiva.10

A VPC15 é intercambiável com a VPC13 em qualquer dose do esquema vacinal, aumentando a imunogenicidade do sorotipo 3, além de adicionar cobertura para os sorotipos exclusivos 22F e 33F.10


Imagem meramente ilustrativa, não reflete o tamanho real do medicamento.

VAXNEUVANCE® é indicada para bebês a partir da sexta semana de vida no esquema de 4 doses, substituindo a VPC13 em qualquer dose do esquema vacinal.10

VAXNEUVANCE® também é indicada para adultos de 18 ou mais no esquema de dose única.10

O esquema posológico em populações especiais deve ser guiado pelas recomendações oficiais e pode incluir mais de uma dose de VAXNEUVANCE.10
VAXNEUVANCE® oferece maior resposta imune contra o sorotipo 3 e proteção adicional contra os sorotipos 22F e 33F.10,12a

Referências: 1. European Centre for Disease Prevention and Control (ECDC). Invasive pneumococcal disease – Facts. 2023. Disponível em: https://www.ecdc.europa.eu/en/pneumococcal-disease/facts. Acessado em 16 de janeiro de 2024. 2. Pelton SI, Weycker D, Farkouh RA et al. Risk of pneumococcal disease in children with chronic medical conditions in the era of pneumococcal conjugate vaccine. Clin Infect Dis. 2014;59(5):615-623. 3. Ministério da Saúde. Situação Epidemiológica das Meningites no Brasil. 2022. Disponível em: https://www.gov.br/saude/pt-br/assuntos/saude-de-a-a-z/m/meningite/publicacoes/situacao-epidemiologica-das-meningites-no-brasil-2022.pdf. Acessado em 18 de janeiro de 2024. 4. European Centre for Disease Prevention and Control (ECDC). Invasive pneumococcal disease – Annual Epidemiological Report for 2018. 2020. Disponível em: https://www.ecdc.europa.eu/en/publications-data/invasive-pneumococcal-disease-annual-epidemiological-report-2018. Acessado em 16 de janeiro de 2024. 5. European Centre for Disease Prevention and Control (ECDC). Surveillance Atlas of Infectious Diseases. Confirmed cases of IPD in children aged <1 year and between 1-4 years: 2014-2019. Disponível em: https://atlas.ecdc.europa.eu/public/index.aspx. Acessado em 16 de janeiro de 2024. 6. Ladhani SN, Collins S, Djennad A, et al. Rapid increase in non-vaccine serotypes causing invasive pneumococcal disease in England and Wales, 2000-17: a prospective national observational cohort study [published correction appears in Lancet Infect Dis. 2018 Feb 6;:]. Lancet Infect Dis. 2018;18(4):441-451. 7. del Amo E, Brotons P, Monsonis M et al. High invasiveness of pneumococcal serotypes included in the new generation of conjugate vaccines. Clin Microbiol Infect. 2014;20(7):684-689. 8. Luck JN, Tettelin H, Orihuela CJ. Sugar-Coated Killer: Serotype 3 Pneumococcal Disease. Front Cell Infect Microbiol. 2020;10:613287. 9. Secretaria de Estado da Saúde de São Paulo. Informação da vigilância das pneumonias e meningites bacterianas. 2021. Disponível em: http://www.ial.sp.gov.br/resources/insituto-adolfo-lutz/publicacoes/sireva_2021_4.pdf. Acessado em 18 de janeiro de 2024. 10. Bula vigente de VAXNEUVANCE. 11. Benfield T, Rämet M, Valentini P et al. Safety, tolerability, and immunogenicity of V114 pneumococcal vaccine compared with PCV13 in a 2+1 regimen in healthy infants: A phase III study (PNEU-PED-EU-2). Vaccine. 2023;41(15):2456-2465. 12. Lupinacci R, Rupp R, Wittawatmongkol O et al. A phase 3, multicenter, randomized, double-blind, active-comparator-controlled study to evaluate the safety, tolerability, and immunogenicity of a 4-dose regimen of V114, a 15-valent pneumococcal conjugate vaccine, in healthy infants (PNEU-PED). Vaccine. 2023;41(5):1142-1152.
As informações requeridas pelo art. 27 da RDC 96/08 dispostas acima são as vigentes até a disponibilização deste material. Acesse a minibula de VAXNEUVANCE clicando aqui
Ressaltamos que VAXNEUVANCE é contraindicada para indivíduos com história de reação alérgica grave (por exemplo, anafilaxia) a qualquer componente da vacina ou a qualquer vacina que contenha toxoide diftérico. Terapias imunossupressoras, incluindo irradiação, antimetabólitos, agentes alquilantes, medicamentos citotóxicos, corticosteroides, proteínas terapêuticas e imunomoduladores direcionados, podem reduzir a resposta imune contra vacinas.
Antes de prescrever o produto, recomendamos a leitura da bula completa para informações detalhadas.
SE PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
Material exclusivo para profissionais de saúde habilitados a prescrever ou dispensar medicamentos.
Copyright © 2024 Merck & Co., Inc., Rahway, NJ, EUA, e suas afiliadas.
Todos os direitos reservados.
BR-PVC-00114 PRODUZIDO EM FEVEREIRO/2024 VÁLIDO POR 6 MESES