Rastreamento e vacinação como estratégias para prevenção do câncer de colo uterino
INTRODUÇÃO
O câncer de colo uterino é um grande problema de saúde pública, sendo que a estimativa mundial aponta que esse tumor foi o quarto mais frequente em todo o mundo em 2018, com uma estimativa de 570 mil novos casos. Sua incidência é maior em países com menor desenvolvimento. Já para o Brasil, o número de novos casos de câncer de colo do útero esperados para cada ano do triênio 2020-2022 será de 16.590 casos.1
De acordo com a Organização Mundial da Saúde (OMS), a eliminação desse câncer depende de múltiplos esforços, incluindo a prevenção por meio da vacinação, rastreamento e tratamento de lesões precursoras, bem como tratamento e cuidados paliativos para o câncer invasivo. Assim, em 2020 essa entidade lançou a Estratégia Global para acelerar a eliminação do câncer de colo do útero como problema de saúde pública, com metas para 2030 que incluem: 90% das meninas totalmente vacinadas contra o papilomavírus humano (HPV) aos 15 anos de idade; 70% das mulheres rastreadas com teste de alto desempenho aos 35 anos de idade e novamente aos 45 anos; 90% das mulheres identificadas com doença cervical (pré-câncer ou câncer invasivo) recebendo tratamento e cuidados.2
Dessa maneira, baseando-se no reconhecimento de que virtualmente todos os casos de câncer de colouterino são atribuíveis à infecção persistente pelo HPV, a prevenção primária desse tumor deve relacionar-se à diminuição do risco de contágio por esse vírus, com programas de orientação à população e vacinação. Em relação à prevenção secundária desse tumor (rastreio), está baseada na premissa de que há progressão do epitélio cervical normal por meio da neoplasia intraepitelial cervical (NIC) para o câncer invasivo. Sabe-se que a triagem citológica isolada como prevenção do câncer de colo uterino foi preconizada por muitos anos, sendo considerada história médica de sucesso. No entanto, diversos estudos vêm sendo publicados na literatura, os quais evidenciaram superioridade de DNA HPV no rastreio desse tumor, tanto isoladamente como associado à citologia.3,4
Relatamos a seguir um caso de câncer de colo uterino que poderia ter sido evitado por meio da vacinação contra o HPV, mas que foi detectado mais precocemente mediante a utilização do teste de DNA HPV.
CASO CLÍNICO
Paciente do sexo feminino, de 45 anos de idade, queixando-se de sinusiorragia e “escapes” no meio do ciclo há 4-5 meses. Negava comorbidades e fumo. Referia uso de galcanezumabe injetável para enxaqueca. Presença de ciclos regulares a cada 28 dias. Parceiro fixo há seis meses com uso de preservativo. Há dez anos apresentou uma gestação com parto normal. O exame físico geral não mostrava alterações, bem como o exame das mamas e da vulva. Ao exame especular visualizava-se colo epitelizado, sem lesões aparentes, com conteúdo fisiológico. Toque vaginal sem alterações e indolor. Nesta consulta foi coletada citologia líquida associada à genotipagem para HPV, exame de reação em cadeia da polimerase (PCR) para clamídia e gonorreia, também foram solicitados exames de rotina (ultrassonografia transvaginal, de mamas e mamografia).
O resultado da citologia cervical mostrou-se negativa para neoplasia, PCR para clamídia e gonorreia negativos, no entanto, o PCR para HPV mostrou positividade para o tipo 16, porém negativo para outros tipos. Em virtude do resultado do exame de DNA HPV a paciente foi convocada para exame de colposcopia. Trouxe resultado de ultrassom transvaginal e de mamas e mamografia sem anormalidades. Na colposcopia apresentava processo inflamatório moderado, com presença de lesão acetobranca densa no interior do canal cervical (Figura 1). Realizada biópsia que evidenciou lesão intraepitelial escamosa de alto grau, não sendo possível excluir invasão estromal.
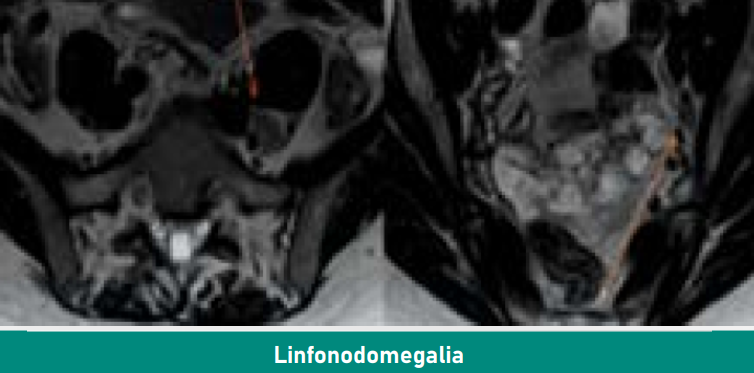
Em virtude desse resultado, solicitou-se ressonância de pelve para melhor avaliação, com os seguintes achados: lesão infiltrativa no estroma do colo uterino (neoplasia primária), com invasão preferencial no quadrante posterior esquerdo, medindo 2,2 x 1,8 cm, estendendo-se até a superfície do colo, sem extensão para os paramétrios; linfonodomegalias suspeitas para natureza secundária: no plano da bifurcação da cadeia ilíaca comum esquerda medindo 2,4 x 1,7 x 1,2 cm; na porção superior da cadeia obturatória esquerda, medindo 1,7 x 0,8 cm (Figura 2).
Mediante os achados anteriores, a paciente foi reavaliada e submetida à nova biópsia do colo que agora confirmou carcinoma escamoso invasivo. A tomografia computadorizada com emissão de posítrons (PET-CT) solicitado mostrou: lesão infiltrativa hipermetabólica no colo uterino; linfonodomegalias com hipermetabolismo acentuado na cadeia obturatória esquerda (0,9 cm) e na ilíaca comum esquerda (1,3 cm). Em virtude do achado de metástase linfonodal, a paciente foi encaminhada pelo oncologista para radioquimioterapia, sendo que apresentou regressão completa da lesão tumoral após tratamento.
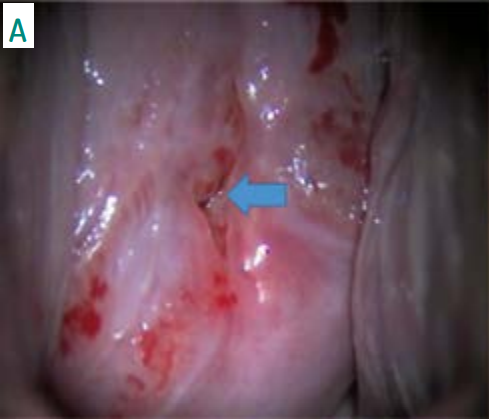
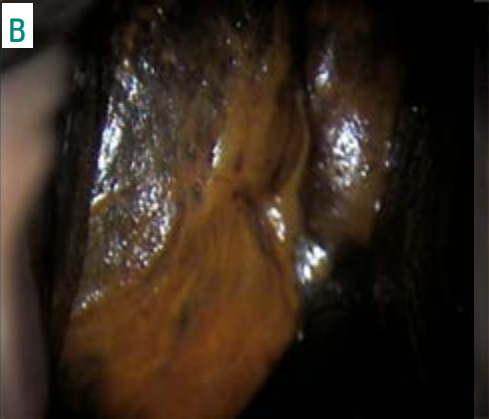
Arquivo pessoal da autora.
Figura 1. Colposcopia onde se evidencia processo inflamatório moderado, com presença de lesão acetobranca densa no interior do canal cervical (seta) (A). Após aplicação de ácido acético e lugol (B).
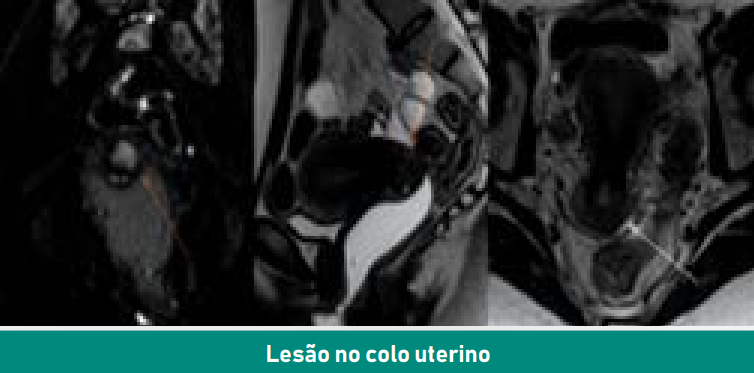
Arquivo pessoal da autora.
Figura 2. Ressonância de pelve.
DISCUSSÃO
O relato apresentado ilustra caso de câncer de colo uterino relacionado ao HPV 16, que infelizmente poderia ter sido evitado por meio da vacinação, mas que foi detectado mais precocemente por meio do teste de DNA HPV. A paciente apresentava exame clínico normal e citologia negativa, no entanto, pela presença do HPV 16 foi indicada colposcopia que detectou o tumor
Apesar de que em nosso país a recomendação do Instituto Nacional de Câncer oriente a citologia como método para rastreamento do câncer de colo uterino, diversas entidades internacionais sugerem que o rastreio com citologia oncológica é preferível para mulheres com idade inferior a 30 anos. Caso se encontre alguma anormalidade citológica, devem- -se seguir as recomendações específicas para esses casos. Para mulheres com mais de 30 anos de idade, é preferível a realização do teste de DNA HPV, apenas para detecção da presença de HPV de alto risco. No entanto, é aceitável a realização do teste conjunto (citologia oncológica associada ao teste de DNA HPV). Caso ambos os testes estejam negativos, devem ser repetido em três a cinco anos. Em casos positivos nos dois exames indica-se colposcopia. Caso se faça opção pelo uso da genotipagem para HPV e o teste mostrar-se positivo para os tipos 16 e 18, mesmo com citologia negativa, deve-se encaminhar para colposcopia.5,6
Em relação à vacinação contra o HPV, apesar dos benefícios, a cobertura vacinal em nosso país é inaceitável.7 De acordo com o Centro de Controle e Prevenção de Doenças (CDC) americano, se os profissionais de saúde aumentassem as taxas de vacinação contra o HPV em receptores elegíveis para 80% na faixa etária alvo, estima-se que 53 mil casos adicionais de câncer de colo uterino poderiam ser evitados durante a vida de mulheres com idade inferior a 12 anos. Além disso, para cada ano em que as taxas de vacinação contra o HPV não aumentam 4.400 mulheres adicionais desenvolverão esse tumor.8
As vacinas contra o HPV estão entre as mais eficazes disponíveis em todo o mundo, com dados inequívocos que demonstram eficácia superior a 99%, quando administradas nas mulheres que não foram expostas aos tipos específicos de HPV. No entanto as mulheres não vacinadas podem receber essas vacinas independente de atividade sexual prévia, exposição anterior ao HPV ou orientação sexual. O teste para DNA de HPV, bem como exames de citologia ou colposcopia não são recomendados antes da vacinação.9
“As vacinas contra o HPV estão entre as mais eficazes disponíveis em todo o mundo, com dados inequívocos que demonstram eficácia superior a 99%”9
Apesar de toda literatura já publicada, muitos médicos ainda têm a ideia equivocada de que se a paciente já apresentou qualquer infecção prévia por HPV, não teriaft
- As pacientes podem não ter adquirido todos os tipos virais contidos nas vacinas e se protegerão contra os tipos com que não haviam se infectado ao recebê-la.10
- A formação de anticorpos na infecção natural pelo HPV não ocorre em todas as mulheres, assim, determinada paciente poderá ter o risco de se infectar novamente pelo mesmo tipo viral que já eliminou. Ao contrário da infecção natural, as vacinas são muito imunogênicas, sendo que a mulher formará anticorpos contra os tipos de HPV contidos nela em aproximadamente 100% casos.11
- Quando uma paciente apresenta verrugas e/ou neoplasia intraepitelial de qualquer localização, essas lesões poderão recidivar apesar do tratamento adequado. Entretanto, alguns estudos têm evidenciado que a administração das vacinas contra o HPV poderia reduzir o risco de recidivas dessas lesões, com benefício na prevenção do aparecimento de novas lesões, que podem ser pelo mesmo sorotipo ou outros.12
CONCLUSÃO
Sabe-se que altas taxas de vacinação contra o HPV reduzirão a carga de doenças relacionadas a esse vírus, no entanto, as taxas de vacinação atuais são inaceitavelmente baixas.7-9 As recomendações dos médicos têm forte influência na aceitação da vacina contra o HPV pelas pacientes e seus pais. Assim, os profissionais de saúde devem recomendar fortemente a vacinação contra o HPV para pacientes elegíveis e enfatizar os benefícios e a segurança dessas vacinas.

Profa. Dra. Adriana Bittencourt Campaner
CRM-SP 75.482
Mestra e Doutora em Tocoginecologia pela Faculdade de Ciências Médicas da Santa Casa de São Paulo (FCMSCSP); Professora Adjunta da FCMSCSP; Médica Chefe do Setor de Patologia do Trato Genital Inferior e Colposcopia do Hospital da Santa Casa de Misericórdia de São Paulo
REFERÊNCIAS
- Ministério da Saúde. Estimativa 2020: incidência de câncer no Brasil. Disponível em: <https://www.inca.gov.br/sites/ ufu.sti.inca.local/files/media/document/estimativa-2020- incidencia-de-cancer-no-brasil.pdf>. Acesso em: jul. 2022.
- World Health Organization. Global strategy to accelerate the elimination of cervical cancer as a public health problem. Geneva: World Health Organization; 2020. Disponível em: <https://www. who.int/publications/i/item/9789240014107>. Acesso em: jul. 2022.
- Quinlan JD. Human papillomavirus: screening, testing, and prevention. Am Fam Physician. 2021;104(2):152-9.
- Bouvard V, Wentzensen N, Mackie A, Berkhof J, Brotherton J, Giorgi-Rossi P, et al. The IARC Perspective on Cervical Cancer Screening. N Engl J Med. 2021;385(20):1908-18.
- Instituto Nacional de Câncer José Alencar Gomes da Silva. Diretrizes brasileiras para o rastreamento do câncer do colo do útero. 2. ed. rev. atual. – Rio de Janeiro: INCA, 2016.114p.
- Fontham ETH, Wolf AMD, Church TR, Etzioni R, Flowers CR, Herzig A, et al, Manassaram-Baptiste D, Saslow D, Wender RC, Smith RA. Cervical cancer screening for individuals at average risk: 2020 guideline update from the American Cancer Society. CA Cancer J Clin. 2020;70(5):321-46.
- Sociedade Brasileira de Imunizações. Coberturas vacinais no Brasil são baixas e heterogêneas, mostram informações do PNI. Disponível em: <https://sbim.org.br/noticias/1359- coberturas-vacinais-no-brasil-sao-baixas-e-heterogeneasmostram-informacoes-do-pni>. Acesso em: jul. 2022.
- Centers for Disease Control and Prevention (CDC). Human papillomavirus vaccination coverage among adolescent girls, 2007-2012, and postlicensure vaccine safety monitoring, 2006-2013 – United States. MMWR Morb Mortal Wkly Rep. 2013;62(29):591-5.
- American College of Obstetricians and Gynecologists’ (ACOG) Committee on Adolescent Health Care, ACOG’ Immunization, Infectious Disease, and Public Health Preparedness Expert Work Group. Human Papillomavirus Vaccination: ACOG Committee Opinion, Number 809. Obstet Gynecol. 2020;136(2):e15-21.
- Dilley S, Miller KM, Huh WK. Human papillomavirus vaccination: Ongoing challenges and future directions. Gynecol Oncol. 2020;156(2):498-502.
- Arbyn M, Xu L, Simoens C, Martin-Hirsch PP. Prophylactic vaccination against human papillomaviruses to prevent cervical cancer and its precursors. Cochrane Database Syst Rev. 2018;5(5):CD009069.
- Bartels HC, Postle J, Rogers AC, Brennan D. Prophylactic human papillomavirus vaccination to prevent recurrence of cervical intraepithelial neoplasia: a meta-analysis. Int J Gynecol Cancer. 2020;30(6):777-82.
Este conteúdo é oferecido pela MSD como um serviço à comunidade médica [aos profissionais de saúde]. Os pontos de vista aqui expressos refletem a experiência e as opiniões dos autores. As informações relacionadas a produto(s) podem ser divergentes das existentes na bula. Antes de prescrever qualquer medicamento eventualmente citado, recomendamos a leitura da bula completa emitida pelo fabricante.
©2022 Planmark Editora EIRELI – Todos os direitos reservados. www.grupoplanmark.com.br O conteúdo desta publicação é de responsabilidade exclusiva de seu(s) autor(es) e não reflete necessariamente a posição da Planmark Editora EIRELI. OS 12348 – set22
Clique aqui para fazer o download da Bula do Profissional
Clique aqui para fazer o download da Bula do Paciente

0800-0122232
online@merck.com
msd.com.br
Copyright © 2022 Merck & Co., Inc., Rahway, NJ, EUA, e suas afiliadas. Todos os direitos reservados
BR-HPV-00729 PRODUZIDO EM AGOSTO/2022 VÁLIDO POR 2 ANOS
