Análise Retrospectiva do Estudo ASPECT-NP
Em uma análise retrospectiva de subgrupos do estudo ASPECT-NP:
ZERBAXA foi uma opção de tratamento efetiva para pacientes com PAH/PAV causadas por Enterobacterales ESBL-positivas ou produtoras de AmpC1
Os resultados de eficácia de ZERBAXA foram comparáveis ao que foi observado em toda população ITT do estudo ASPECT-NP¹
Mortalidade por todas as causas no dia 28
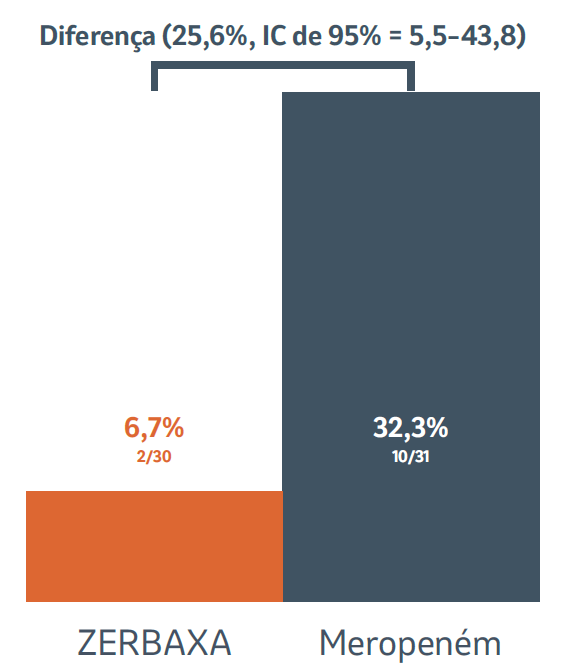
Adaptado de: Paterson DL et al.¹
Taxa de cura clínica
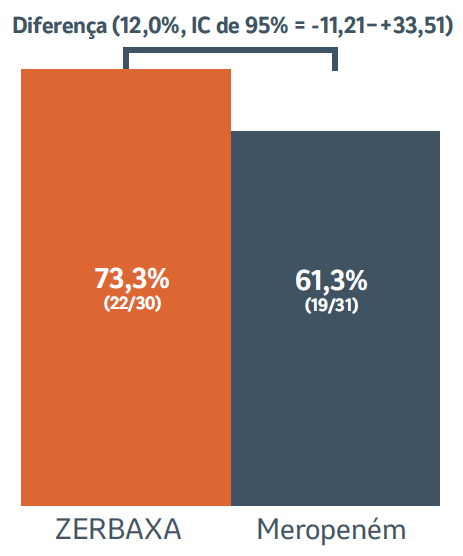
Adaptado de: Paterson DL et al.¹
- A cura clínica e a taxa de resposta microbiológica foram similares entre os braços de tratamento para isolados de Enterobacterales ESBLpositivas ou produtoras de AmpC, independentemente do patógeno basal do trato respiratório inferior¹
| ZERBAXA (% [n/N]) | Meropeném (% [n/N]) | Diferença (%, IC de 95%) | |
|---|---|---|---|
| Taxa de cura clínica | 73,3 (22/30) | 61,3 (19,31) | 12,0 (-11,2, 33,5) |
| Resposta microbiológica por patógeno | 64,5 (20/31) | 74,3 (26/35) | -9,8 (-30,8, 12,0) |
ESBL: β-lactamase de espectro estendido; ITT: com intenção de tratamento.
- O ASPECT-NP foi um estudo de fase 3, randomizado, controlado, duplo-cego, multicêntrico e de não inferioridade, que comparou ZERBAXA com meropeném no tratamento de pacientes com PAH/PAV.¹
- Essa análise post hoc retrospectiva do estudo ASPECT-NP incluiu todos os participantes randomizados que apresentaram ≥ 1 isolado basal de Enterobacterales no trato respiratório inferior, que fossem ESBL-positivas e/ ou produtoras de AmpC, e que não fossem positivas para carbapenemases. Todos os patógenos basais do trato respiratório inferior deveriam ser suscetíveis aos dois medicamentos do estudo.¹
- Características clínicas basais, patógenos e suscetibilidade a agentes antibacterianos fora do estudo foram geralmente comparáveis entre os braços de tratamento.¹
- Essas análises foram de natureza exploratória e retrospectiva, não tinham poder para detectar diferenças significativas e, assim, devem ser interpretadas com cuidado devido ao pequeno tamanho da amostra e à baixa taxa de eventos clínicos.¹
- O estudo ASPECT-NP não tinha poder para avaliação de não inferioridade de ZERBAXA em nenhuma subpopulação.¹
- Essas análises utilizaram o ponto de corte de suscetibilidade provisório de 4 mg/L para ZERBAXA, para que fossem consistentes com o protocolo e as análises publicadas anteriormente, mas o ponto de corte de suscetibilidade do CLSI e do EUCAST para Enterobacterales foi definido como 2 mg/L.¹
- Devido aos dados insuficientes sobre a concentração plasmática no subgrupo ESBL/AmpC, o impacto potencial dos níveis de tazobactam nos desfechos do tratamento na análise não foi avaliado.¹
CLSI: Clinical and Laboratory Standards Institute; ESBL: betalactamase de espectro estendido; EUCAST: European Committee on Antimicrobial Susceptibility Testing; IC: intervalo de confiança; ITT: intenção de tratar; PAH: pneumonia adquirida no hospital; PAV: pneumonia associada à ventilação.
Referência
- Paterson DL, Bassetti M, Motyl M et al. Ceftolozane/tazobactam for hospital-acquired/ventilator-associated bacterial pneumonia due to ESBL-producing Enterobacterales: a subgroup analysis of the ASPECT-NP clinical trial. J Antimicrob Chemother. 2022;77(9):2522-2531.
Clique aqui para acessar a minibula
As informações requeridas pelo art. 27 da RDC 96/08 dispostas acima são as vigentes até a disponibilização deste material. Elas estão sujeitas a alterações posteriores, portanto, caso queira consultar a versão vigente após o recebimento do conteúdo clique aqui.
Ressaltamos que ZERBAXA é contraindicado para pacientes com hipersensibilidade a qualquer agente antibacteriano cefalosporínico e hipersensibilidade grave (p. ex., reação anafilática ou reação cutânea grave) a qualquer um dos tipos de agente antibacteriano betalactâmico (p. ex., penicilinas ou carbapenéns). Não são previstas interações medicamentosas com ZERBAXA e substratos, inibidores e indutores das enzimas do citocromo P-450 com base em estudos in vivo e in vitro.
Antes de prescrever o produto, recomendamos a leitura da bula completa para informações detalhadas.
SE PERSISTIREM OS SINTOMAS, O MÉDICO DEVERÁ SER CONSULTADO.
Material exclusivo para profissionais de saúde habilitados a prescrever ou dispensar medicamentos.
Copyright © 2023 Merck & Co., Inc., Rahway, NJ, EUA, e suas afiliadas.
Todos os direitos reservados.
BR-ZER-00435 PRODUZIDO EM ABRIL/2023 VÁLIDO POR 2 ANOS
