KEYTRUDA®, em combinação com carboplatina e paclitaxel ou nab-paclitaxel para tratamento de primeira linha em pacientes com CPCNP escamoso e metastático.1
Desenho do estudo KEYNOTE-407
Estudo de fase 3, randomizado, multicêntrico, duplo-cego e controlado com placebo em 559 pacientes não tratados previamente com CPCNPm escamoso, independentemente do status de expressão tumoral de PD-L1.2
Estudo de fase 3 em pacientes com CPCNPm escamoso (n=559)1,2
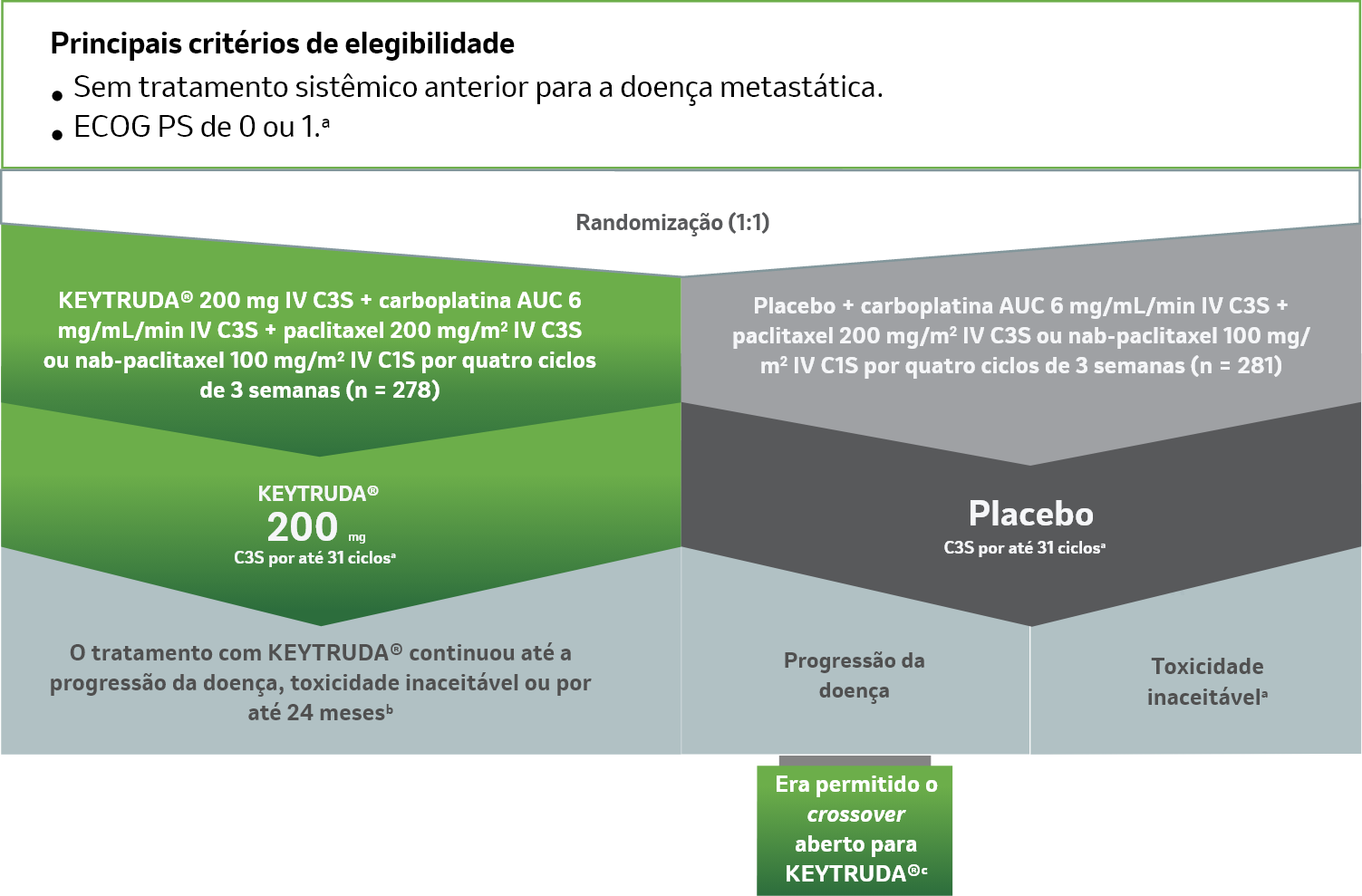
aSegundo Paz-Ares L, Luft A, Vicente D, et al, para os investigadores do KEYNOTE-407. Pembrolizumab plus chemotherapy for squamous non-small-cell lung cancer. N Engl J Med. 2018;379(21):2040-2051.
bFoi permitida a administração de KEYTRUDA® para além da progressão da doença definida por RECIST caso o paciente estivesse clinicamente estável e o investigador considerasse que haveria benefício clínico.2
cApenas os pacientes no grupo de quimioterapia que apresentaram progressão da doença verificada por BICR segundo RECIST v1. poderiam fazer o crossover para receber KEYTRUDA® como monoterapia.2
- Objetivos primários de eficácia: sobrevida global (SG) e sobrevida livre de progressão (SLP), avaliadas por BICR segundo os critérios RECIST v1.1, modificados para acompanhar no máximo 10 lesões-alvo no total e no máximo 5 lesões-alvo por órgão.2,3
- Objetivos secundarios de eficácia: TRO e DR, avaliadas por BICR segundo os critérios RECIST v1.1, modificados para acompanhar no máximo 10 lesões-alvo no total e no máximo 5 por órgão.2,3
- Os pacientes foram estratificados conforme o status tumoral de PD-L1 (PPT < 1% vs. PPT ≥ 1%), tipo de taxano utilizado (paclitaxel ou nab-paclitaxel) e região geográfica (Ásia Oriental vs. não Oriental).2
- Pacientes com doença autoimune com necessidade de tratamento sistêmico nos 2 anos anteriores, condição médica com necessidade de imunossupressão ou que haviam recebido mais de 30 Gy de radiação torácica nas 26 semanas anteriores não foram considerados elegíveis.1-3
Características dos pacientes do KEYNOTE-407
Um total de 559 pacientes foi distribuído de forma randomizada: 278 pacientes para o grupo de KEYTRUDA® e 281 para grupo de placebo. As características da população do estudo foram: mediana de idade de 65 anos (intervalo: 29 a 88); 55% de 65 anos ou mais; 81% homens; 77% brancos; ECOG PS de 0 (29%) e 1 (71%); e 8% com metástases cerebrais tratadas no início do estudo. Trinta e cinco por cento tinham expressão tumoral de PD-L1 com PPT < 1% [negativo]; 19% eram da região da Ásia oriental; e 60% receberam paclitaxel.1,2
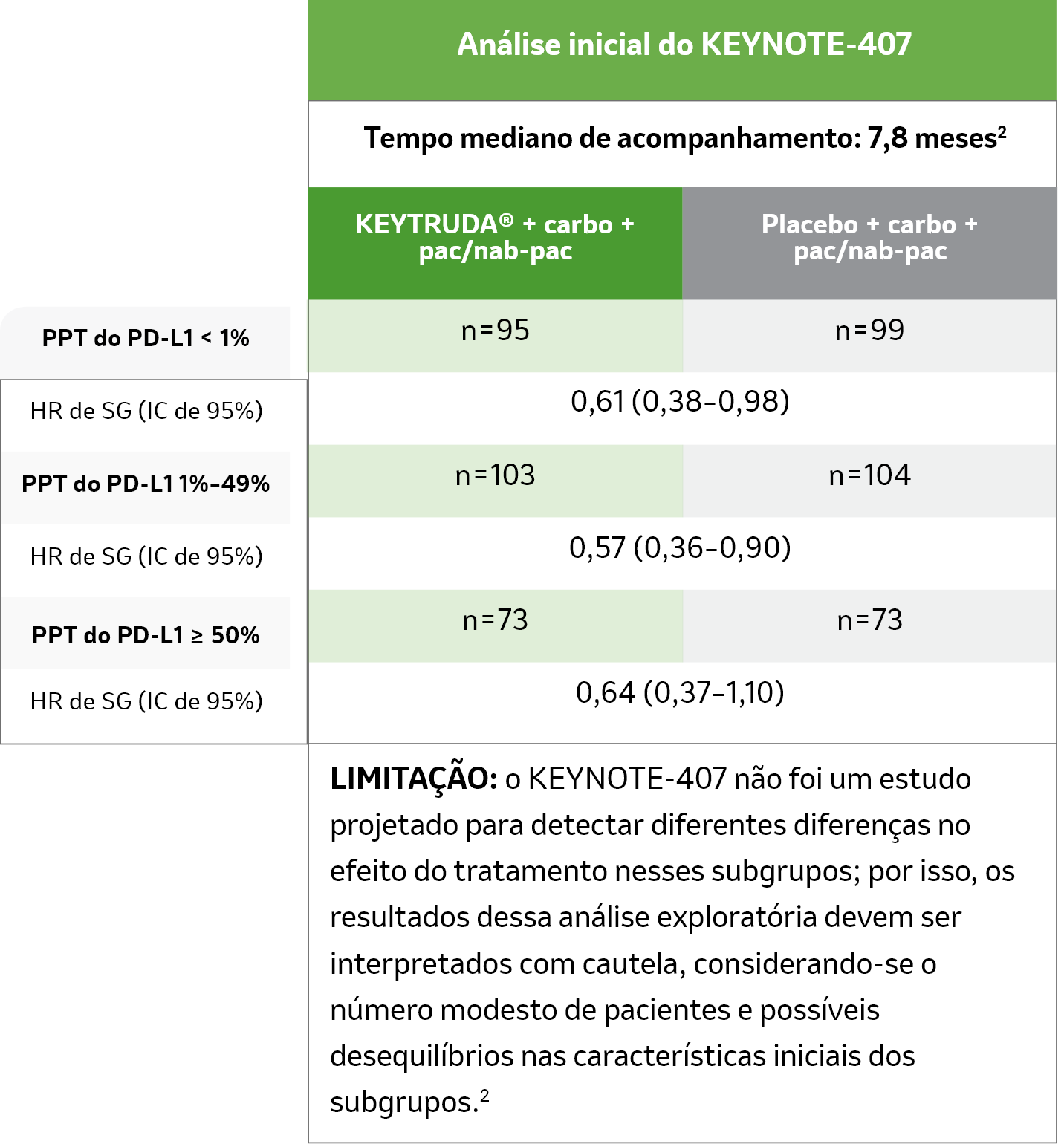
Análise interina do KEYNOTE-407
Tempo mediano de acompanhamento: 7,8 meses2
-
SG superior: KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac.2,a
- 36% de redução de risco de morte com KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac (HR = 0,64; IC de 95%: 0,49–0,85; P < 0,001)2,b
- SG mediana: 15,9 meses (IC de 95%: 13,2-NA) com KEYTRUDA® + carbo + pac/nab-pac vs. 11,3 meses (IC de 95%: 9,5-14,8) com carbo + pac/nab-pac.2
- Eventos: 30,6% (85/278) com KEYTRUDA® + carbo + pac/nab-pac e 42,7% (120/281) com carbo + pac/nab-pac.4
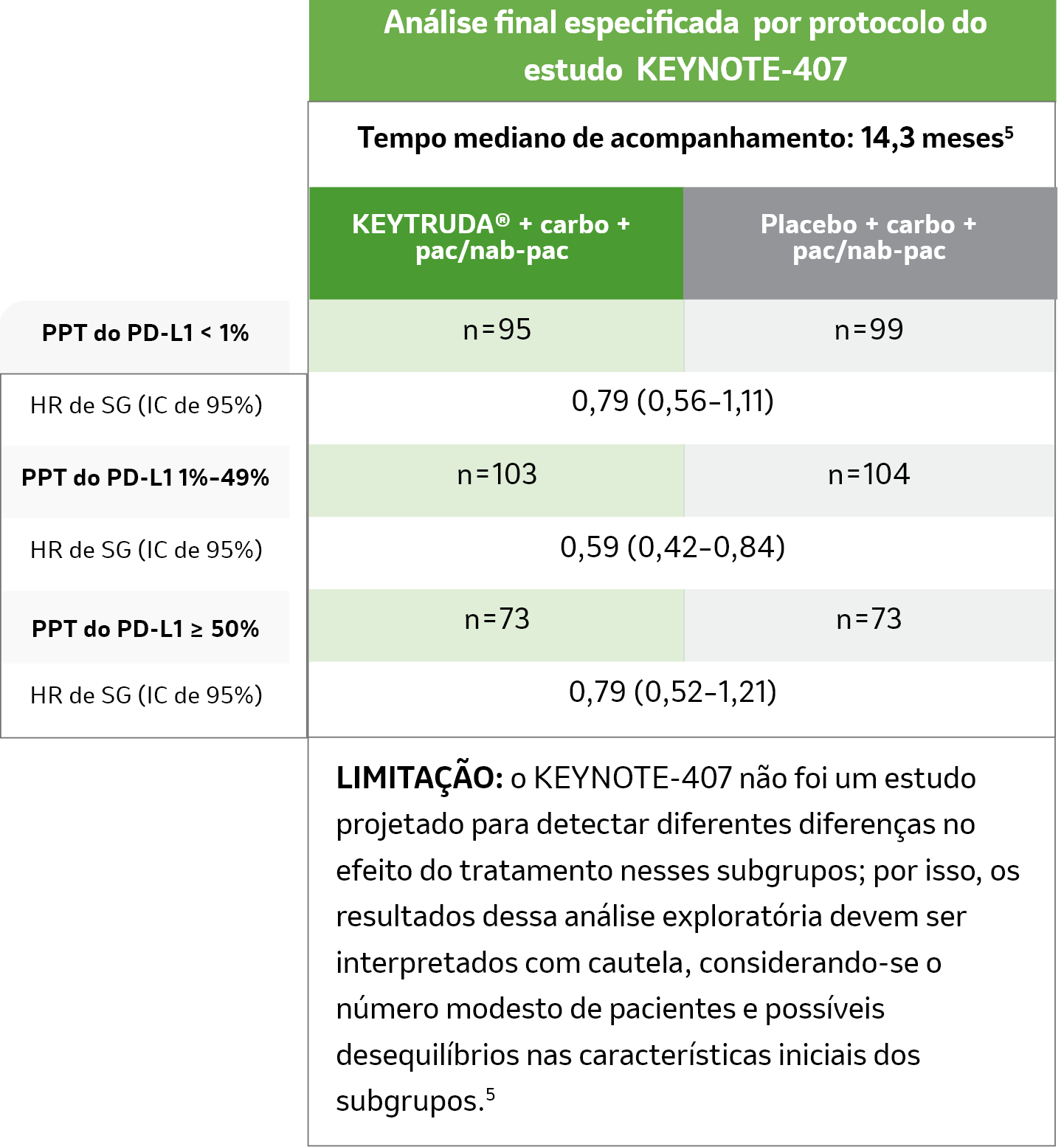
Análise final especificada por protocolo do KEYNOTE-407
Tempo mediano de acompanhamento: 14,3 meses1,5
-
SG duradoura: KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac.
- HR= 0,71 (IC de 95%: 0,58-0,88).1,5
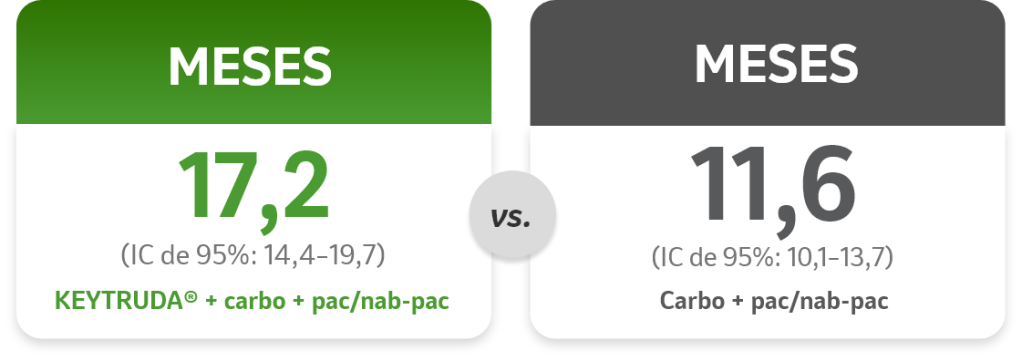
- SG mediana: 17,1 meses (IC de 95%: 14,4–19,9) com KEYTRUDA® + carbo + pac/nab-pac vs. 11,6 meses (IC de 95%: 10,1–13,7) com carbo + pac/nab-pac.1,5
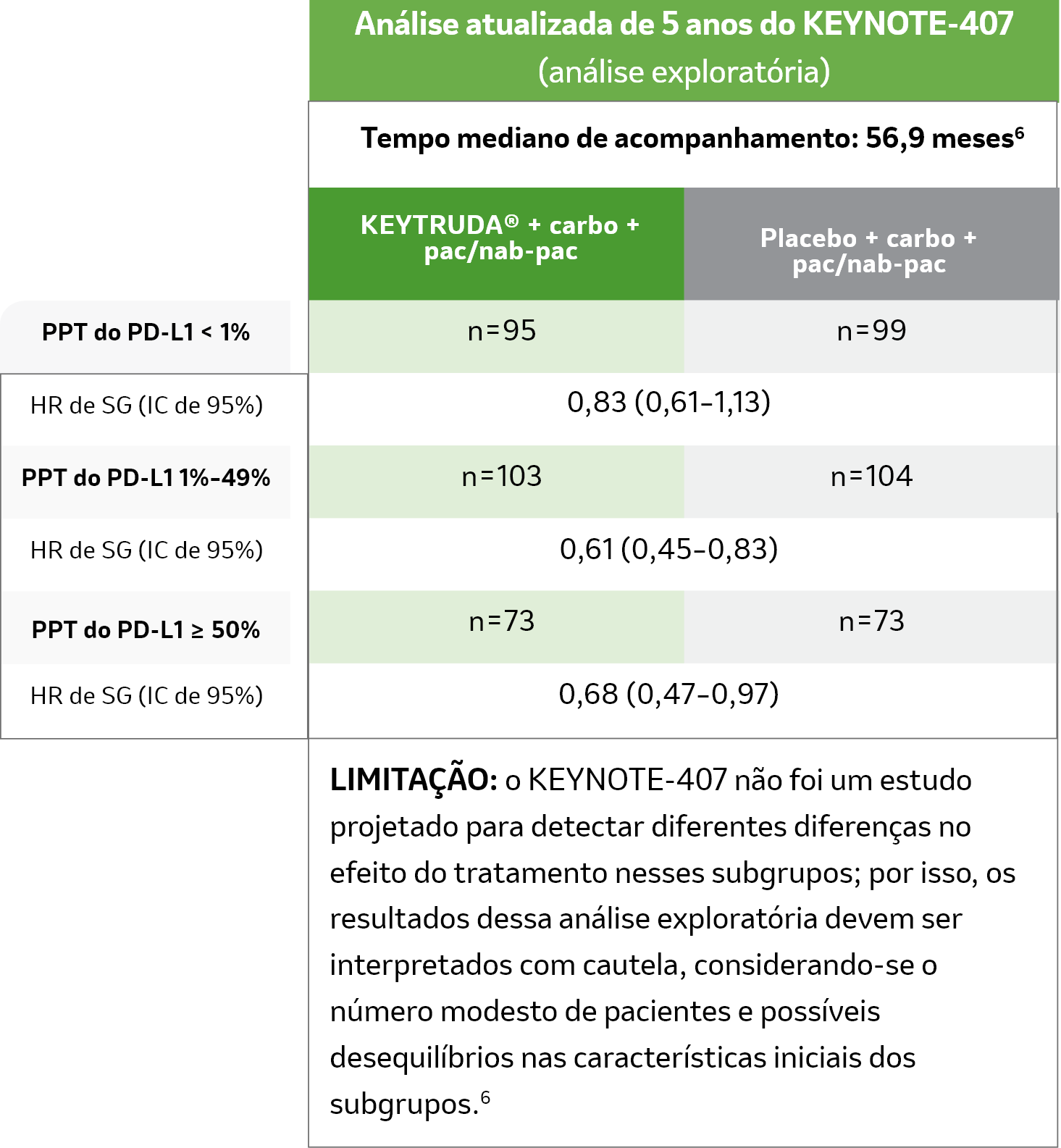
Análise atualizada de 5 anos do KEYNOTE-407 (análise exploratória)
Tempo mediano de acompanhamento: 56,9 meses6
SG: KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac6,c
LIMITAÇÃO: Esta análise post-hoc (acompanhamento mediano: 56,9 mesesc) no KEYNOTE-407 foi de natureza exploratória e realizada após a análise final especificada pelo protocolo. Não foi planejado nenhum teste formal para esta análise, portanto, não se pode tirar conclusões estatísticas. Os participantes do estudo, de qualquer um dos grupos, poderiam receber tratamento posterior contra o câncer.6
TAXA DE CROSSOVER: 50,9% – 117 pacientes passaram para monoterapia com KEYTRUDA® durante o estudo, e outros 26 receberam tratamento anti-PD-(L)1 após o término do estudo.6,d
aTempo desde a randomização até a morte ou a data de corte dos dados para aqueles que estavam vivos.2
bHR com base no modelo de risco proporcional de Cox estratificado; valor de p com base em um teste log-rank estratificado.2
cTempo desde a randomização até a data de corte dos dados.6
dAnti–PD-L1 ou anti–PD-1.
SG com KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac (análise exploratória)6,c
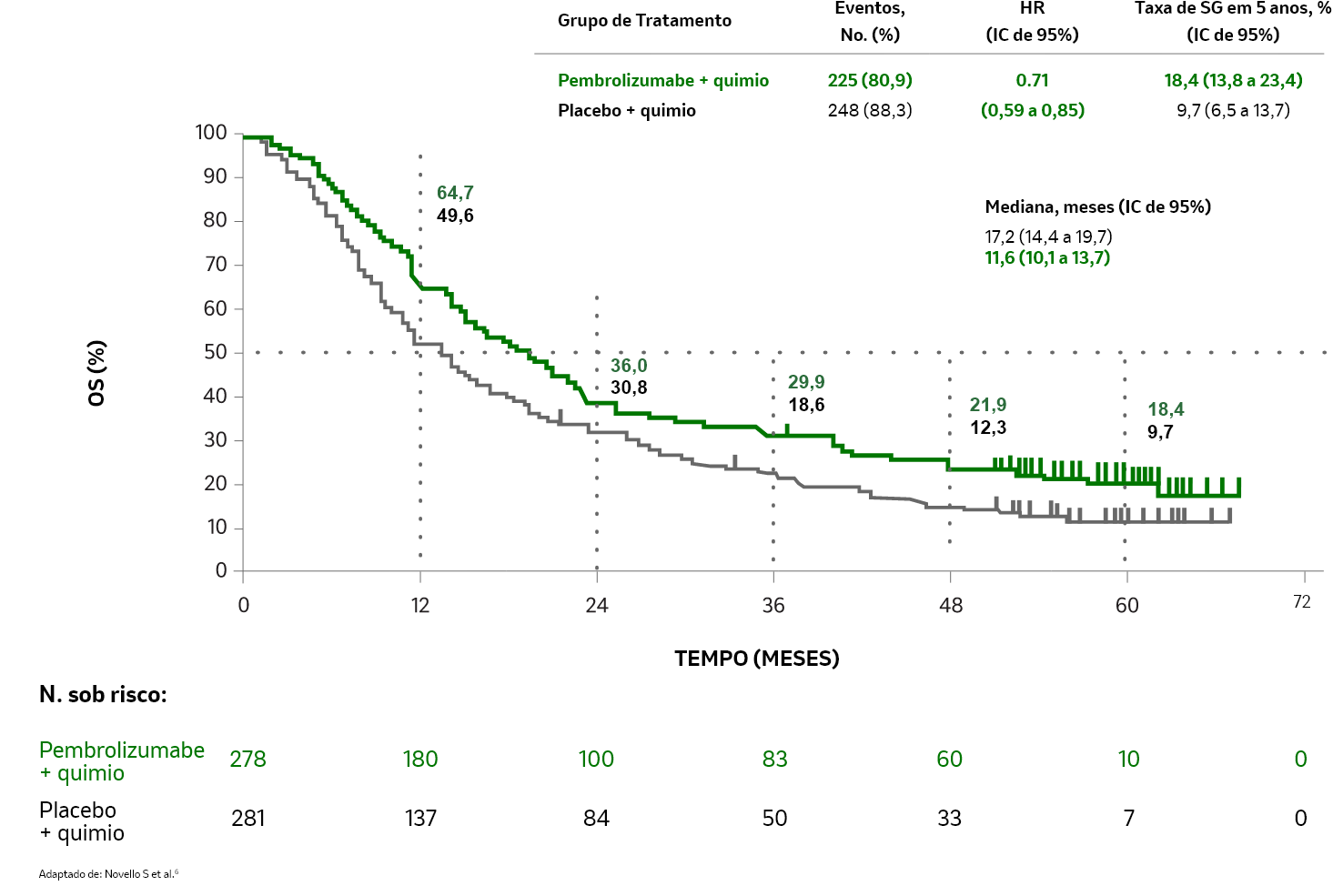
SG mediana6
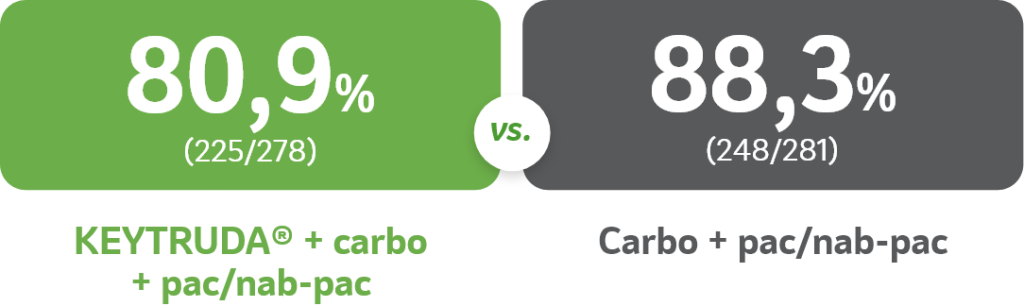
Eventos6
Análise interina do KEYNOTE-407
Tempo mediano de acompanhamento: 7,8 meses2
-
SLP superior:2
- Redução de 44% no risco de progressão da doença ou morte com KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac (HR = 0,56; IC de 95%: 0,45–0,70; P< 0,001).2,a
- SLP mediana: 6,4 meses (IC de 95%: 6,2–8,3) com KEYTRUDA® + carbo + pac/nab-pac vs. 4,8 meses (IC de 95%: 4,3–5,7) com carbo + pac/nab-pac.2
- Eventos: 54,7% (152/278) com KEYTRUDA® + carbo + pac/nab-pac vs. 70,1% (197/281) com carbo + pac/nab-pac.4
Análise final especificada por protocolo do KEYNOTE-407
Tempo mediano de acompanhamento: 14,3 meses1,5
- Redução de 43%: no risco de progressão da doença ou morte com KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac (HR = 0,57; IC de 95%, 0,47-0,69).2,5
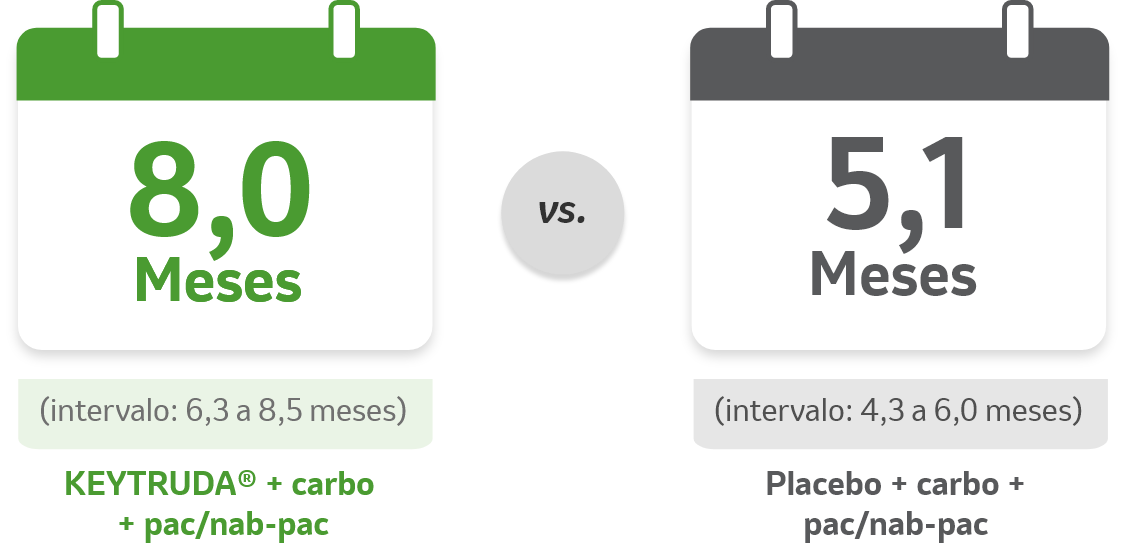
- SLP mediana: 8,0 meses (IC de 95%, 6,3–8,4) com KEYTRUDA® + carbo + pac/nab-pac vs. 5.1 meses (IC de 95%, 4.3–6) com placebo + carbo + pac/nab-pac.1,5
Análise atualizada de 5 anos do KEYNOTE-407 (análise exploratória)
Tempo mediano de acompanhamento: 56,9 meses6
SLP: KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac6,b
LIMITAÇÃO: Esta análise post-hoc (acompanhamento mediano: 59,9 meses) do KEYNOTE-407 foi de natureza exploratória e realizada após a análise final especificada pelo protocolo. Não foi planejado nenhum teste formal para esta análise, portanto, não se pode tirar conclusões estatísticas.6
aHR com base no modelo de risco proporcional estratficado de Cox; valor de p com base em teste logarítmico estratificado.2
bSegundo critérios RECIST v1.1 por BICR.6
SLP: KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac6,b
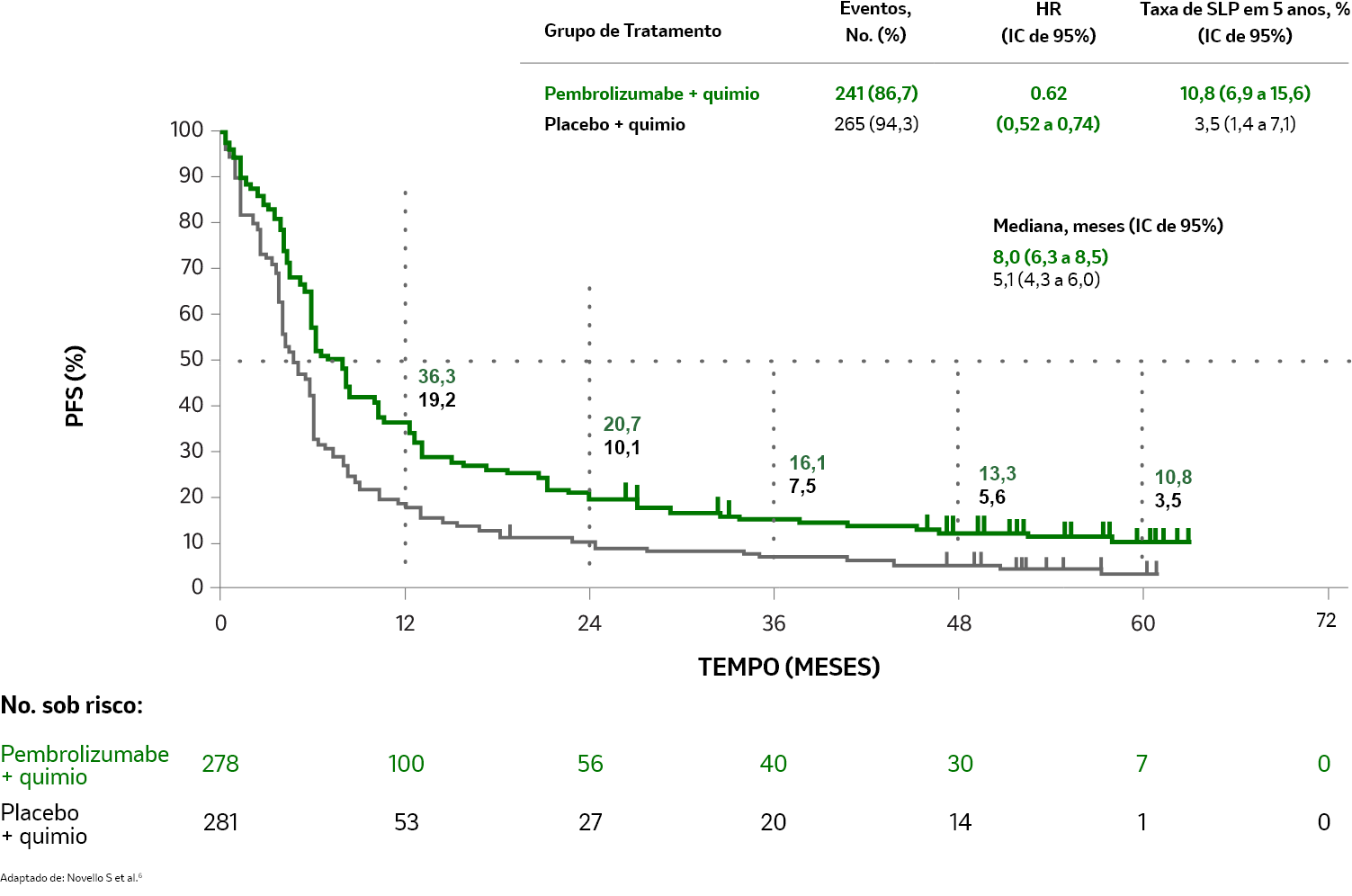
SLP mediana6,b
Eventos6,b

Análise interina do KEYNOTE-407
Tempo mediano de acompanhamento: 7,8 meses2
-
TRO estatisticamente significativa2
- 57,9% (IC de 95%, 51,9-63,8) com KEYTRUDA® + carbo + pac/nab-pac vs. 38,4% (IC de 95%: 32,7-44,4) com carbo + pac/nab-pac; P=0,0004.
- DR mediana: 7,7 meses (intervalo: 1,1+ a 14,7+) com KEYTRUDA® + carbo + pac/nab-pac vs. 4,8 meses (intervalo: 1,3+ a 15,8+) com carbo + pac/nab-pac.2
Análise final especificada por protocolo do KEYNOTE-407
Tempo mediano de acompanhamento: 14,3 meses.1,5
- TRO: 62,6% com KEYTRUDA® + carbo + pac/nab-pac vs. 38,4% com carbo + pac/nab-pac.1,5
- DR mediana: 8,8 meses (intervalo: 1,3+ a 28,4+) com KEYTRUDA® + carbo + pac/nab-pac vs. 4,9 meses (intervalo: 1,3+ a 28,3+) com carbo + pac/nab-pac.1,5
Análise atualizada de 5 anos do KEYNOTE-407 (análise exploratória)
Tempo mediano de acompanhamento: 56,9 meses6
TRO: quase dois terços dos pacientes responderam a KEYTRUDA® + carbo + pac/nab-pac vs. carbo + pac/nab-pac6,a
LIMITAÇÃO: Esta análise post-hoc (acompanhamento mediano: 56,9 meses) do KEYNOTE-407 foi de natureza exploratória e realizada após a análise final especificada pelo protocolo. Não foi planejado nenhum teste formal para esta análise, portanto, não se pode tirar conclusões estatísticas.6
TRO6

a Segundo critérios RECIST v1.1 avaliados por BICR.6
b Estimativas de Kaplan-Meier. Data de corte dos dados: 23 de fevereiro de 2022.6
Mediana de DR no momento da análise atualizada6,b

a Segundo RECIST versão 1.1 por BICR.4
c Estimativa de Kaplan-Meier. Data de corte dos dados: 8 de março de 2022.4
Você pode recomendar aos seus pacientes adequados que não expressam PD-L1: “Temos a opção de começar com KEYTRUDA® + quimioterapia.”2
Referencias: 1. Bula vigente de KEYTRUDA®. 2. Paz-Ares, Lu A, Vincente D et al. Pembrolizumab plus chemotherapy for squamous non–small-cell lung cancer. N Engl J Med. 2018;379(21):204 –2051. 3. Paz-Ares L, Lu A, Vicente D et al. Pembrolizumab plus chemotherapy for squamous non-small-cell lung cancer. N Engl J Med. 2018;379(21):2040–2051. 4. Paz-Ares L, Luft A, Vicente D et al. Supplementary appendix to: Pembrolizumab plus chemotherapy for squamous non-small-cell lung cancer. N Engl J Med. 2018;379(21):2040–2051. 5. Paz-Ares L, Vicente D Tafreshi A et al. A randomized, placebo-controlled trial of pembrolizumab plus chemotherapy in patients with metastatic squamous NSCLC: protocol-specified final analysis of KEYNOTE-407. J Thorac Oncol. 2020;15(10):1657-1669. 6. Novello S, Kowalski DM et al. Pembrolizumab Plus Chemotherapy in Squamous Non-Small-Cell Lung Cancer: 5 Year Update of the Phase III KEYNOTE-407 Study. J Clin Oncol.2023;41(11):1999-2006.
Abreviaturas: ALK = quinase de linfoma anaplásico; AUC = área sob a curva; BICR = revisão central independente e cega; C3S = a cada 3 semanas; CPCNP = câncer de pulmão de células não pequenas; CPCNPm = câncer de pulmão de células não pequenas metastático; DR = duração da resposta; ECOG PS = performance status do Eastern Cooperative Oncologic Group; EGFR = receptor do fator de crescimento epidérmico; HR = razão de risco; IC = intervalo de confiança; NA = não alcançado; PD-1 = receptor de morte programada 1; PD-L1 = ligante 1 de morte programada; plat/pem = carboplatina ou cisplatina e pemetrexede; PPT = pontuação de proporção do tumor; RC = resposta completa; RECIST v1.1 = Critérios de Avaliação de Resposta em Tumores Sólidos v1.1; RP = resposta parcial; SG = sobrevida global; SLP = sobrevida livre de progressão; TRO = taxa de resposta objetiva.